干细胞治疗肝纤维化、肝硬化的临床研究进展
对于肝纤维化或肝硬化来说,既经济又有效的治疗方案很少。许多研究干细胞治疗肝病的临床试验表明,干细胞有可能成为一种治疗途径。本综述旨在整合已发表的干细胞治疗肝纤维化/肝硬化的临床试验信息,提供不同细胞来源、剂量和递送方法的最新概述,以及讨论了各种干细胞在临床应用中的优势和局限性。此外,本文还研究了干细胞有助于治疗肝纤维化的分子机制,包括肝再生、免疫调节、损伤抵抗、肌成纤维细胞抑制和细胞外基质降解。
全球每年约有200万人死于肝病,占每年总死亡人数的3.5%。其中,有100万人死于肝硬化引起的并发症。肝硬化是全球第11大最常见的死亡原因,预计全球死亡的绝对数量和比例都将上升。2017年,肝硬化导致的死亡人数超过132万,而1990年的死亡人数不到89.9万。慢性肝病的进展分为四个阶段:炎症、肝纤维化、肝硬化和终末期肝病(ESLD)或肝癌。这种序列常常导致肝功能的不可逆损害,而正异性肝移植(OLT)是唯一的治疗方法。然而,OLT面临着免疫排斥、术后并发症和器官短缺等重大挑战,促使人们探索替代治疗方法。
细胞治疗的概念在1976年获得了动力,首次临床前治疗的原代人肝细胞(phh)。虽然phh被认为是治疗代谢性肝病的理想来源,并已进入临床应用,但其有限的可用性和体外扩增的挑战导致了对替代细胞来源的探索。
干细胞治疗脱颖而出,在治疗肝纤维化和肝硬化的I期和II期临床试验中显示出有效性,已成为一种有前景的途径。
与人类原代干细胞相关的问题限制了临床试验的数量,因此必须依赖动物模型进行安全性和有效性测试。动物模型在证明干细胞疗法的有效性、可行性和安全性方面发挥了至关重要的作用。尽管啮齿动物模型与人类疾病存在差异,但它们是从基础研究到临床应用的重要桥梁。干细胞治疗机制包括分化为功能性细胞以替代受损细胞,以及产生生物活性因子以增强组织驻留祖细胞的增殖、成熟和免疫调节。后一种途径被认为特别有效,通过基质金属蛋白酶(MMP)和组织金属蛋白酶抑制剂(TIMP)等细胞外基质(ECM)重塑介质促进炎症调节和纤维化逆转。
与外科手术方法相比,基于干细胞的治疗提供了一种侵入性较小的选择,免疫排斥风险低。本综述全面总结了利用干细胞治疗肝纤维化和肝硬化的最新临床进展,旨在为干细胞治疗的未来临床转化提供见解。
肝硬化和纤维化干细胞治疗的进展
在用干细胞治疗肝硬化和纤维化领域,对clinicaltrials.gov的全面搜索显示,有160项针对肝脏疾病的注册临床试验,其中75项(47%)专门针对肝硬化或纤维化。这些试验大部分(36%)处于I/II期。值得注意的是,间充质干细胞(MSCs)是使用的主要细胞类型,占病例的73%,其来源多种多样。脐带来源的MSCs显示出优越的有效性。输注途径主要选择经肝动脉输注(32%)。
在细胞剂量方面,治疗至少需要100万个细胞,实际剂量取决于患者体重、临床状况、给药途径和细胞类型等因素。对于肝硬化或肝功能衰竭,肝细胞治疗的目标是为受损的肝脏提供功能支持,细胞计数约为理论肝肿块的10-15%。门静脉高压和细胞栓塞等并发症限制了输注的细胞数量。
给药途径是干细胞悬液输注还是生物工程干细胞制品移植,这是一个关键的考虑因素。目前,肝动脉输注是首选途径,可能是因为与静脉输注相比,肝动脉输注具有更好的植入性。值得注意的是,只有一项临床试验使用了生物工程产品,一种可注射的胶原支架与人类脐带间充质干细胞相结合。
评估细胞疗法的安全性和有效性是至关重要的。干细胞,特别是间充质干细胞,在肝硬化或肝纤维化治疗的临床试验中显示出有希望的进展。常用的评价指标包括血清白蛋白水平、血清胆红素、Child-Pugh评分和MELD评分。安全性评估基于术后不良并发症,尽管仍有必要进行更大规模的研究以获得更全面的了解。
用于肝纤维化/肝硬化治疗的干细胞类型
探索干细胞治疗肝脏疾病的临床试验,特别是肝硬化和纤维化,揭示了具有不同特征的多种细胞类型。下面我们就来深入了解一下这些干细胞类型:
间充质干细胞(Mesenchymal Stem Cells,间充质干细胞):广泛应用并来源于各种组织,间充质干细胞具有特定的特征(CD73, CD90, CD105阳性;CD34、CD14、CD11b、CD79、CD19, HLA-DR阴性)。
脐带间充质干细胞(UCMSCs): UCMSCs从脐带血中分离出来,经酶消化或外植体法处理,具有很强的免疫抑制能力,促进肝脏修复。
优势和局限性:干细胞来源的比较分析揭示了、增殖和免疫原性的差异。每种来源都有独特的优势和挑战,强调在临床应用中需要仔细考虑。同种异体UCMSCs的再生能力以及LDMSCs的肝脏特异性环境值得注意。造血干细胞、BMMNCs和EPCs表现出异质性,使其临床应用复杂化。理想的来源仍然难以捉摸,需要对标准化方案和更广泛的临床验证进行持续研究。
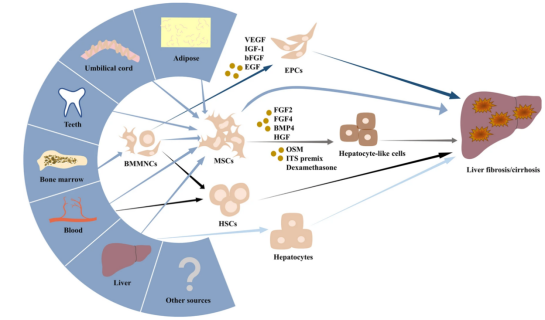
肝纤维化的过程包括肝细胞死亡、免疫细胞浸润、肝损伤、肌成纤维细胞活化和过度的细胞外基质沉积等关键事件。本文探讨了干细胞治疗在解决这些方面的机制。间充质干细胞(MSCs)是公认的多能性和增殖能力。然而,现在人们了解到它们的再生潜力在于旁分泌作用而不是分化。
干细胞通过三种主要机制促进肝脏再生。首先,它们迁移到肝脏并转分化为肝细胞。趋化因子配体12 (CXCL12)在向肝脏募集间充质干细胞中起着至关重要的作用。CXCL12的浓度梯度影响干细胞迁移,CXCR7促进肝脏再生,而CXCR4促进纤维化。在归巢到受损肝脏后,肝脏特异性细胞外基质通过整合素途径诱导间充质干细胞发生肝。
其次,干细胞通过释放激活信号通路的细胞因子来促进肝细胞增殖。间充质干细胞增加血清IGF-1水平,IGF-1作用于IGF1R,上调PI3K/AKT通路。msc培养基诱导与肝细胞增殖相关的细胞因子的表达。AKT是细胞生长的关键参与者,它被激活,通过AKT/β-Catenin通路改善葡萄糖合成和增强肝细胞增殖。
第三,干细胞有助于血管生成,这是肝脏再生所必需的过程。msc衍生因子上调促血管生成因子和受体,促进微血管再生。VEGF-A信号通过增加血供和释放旁分泌因子,促进肝细胞增殖。
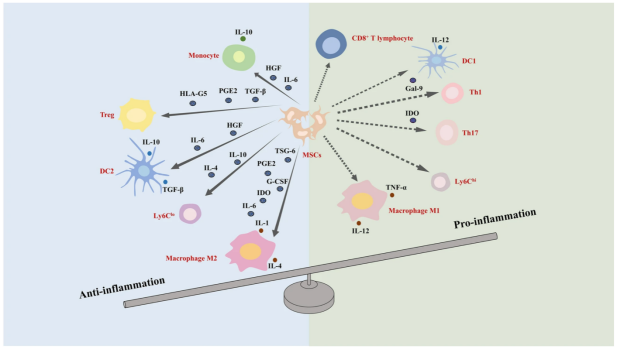
在免疫调节方面,间充质干细胞通过转化免疫细胞产生免疫抑制微环境。间充质干细胞抑制单核细胞分化,使巨噬细胞极化向抗炎表型倾斜,并调节树突状细胞分化。此外,间充质干细胞抑制CD4+和CD8+
T淋巴细胞的激活和增殖,诱导调节性T细胞,并分泌IL-2受体作为诱饵抑制IL-2活性。
总体而言,肝纤维化的干细胞治疗涉及复杂的机制相互作用,包括迁移和转分化、肝细胞增殖、血管生成促进以及通过调节各种免疫细胞类型进行免疫调节。
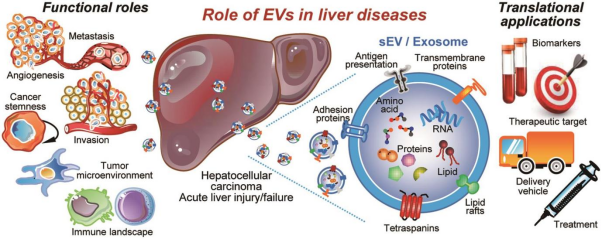
肝纤维化治疗与细胞外囊泡机制
肝纤维化是由慢性损伤引起的,受到各种分子的影响,如促炎因子、氧化应激产物、凋亡介质和细胞因子。间充质干细胞(MSC)通过提供抗炎、抗氧化和抗凋亡作用显示出治疗益处。
抗炎特性:MSC通过下调IFN-γ/Stat1和IL-6/Stat3信号通路,降低促炎因子(TNF-α、IFN-γ、IL-6、IL-1β、TGF-β1、IL-4)。过表达HNF-4α的MSC通过激活NF-κB通路,增强iNOS表达,发挥抗炎作用。
抗氧化作用:MSC通过分泌抗氧化酶(SOD、GPx、CAT、HO-1、GSH),恢复正常线粒体功能,并通过Nrf2/HO-1通路诱导抗氧化反应,减少氧化应激介质。各种MSC类型减少丙二醛(MDA),脂质过氧化的产物,并增强线粒体功能。
抗凋亡活性:MSC-Exos和hUCMSCs通过依赖pink1的线粒体自噬途径和保护性自噬体的产生减少肝细胞凋亡。Ly6Clo巨噬细胞通过PtdSer/MerTK/ERK轴吞噬凋亡小体,MSC-Exos降低凋亡相关蛋白的表达。
抑制肌成纤维细胞活性:间充质干细胞通过下调TGF-β I型受体(TGFBR1)、降低SMAD2的磷酸化和降低Wnt通路相关蛋白来抑制肌成纤维细胞的激活。间充质干细胞通过抑制LPS/TLR4通路和诱导巨噬细胞表型转换来降低肌成纤维细胞活性。
细胞外基质降解与重塑:间充质干细胞通过下调TGF-β1/SMAD3和TGFBR1,促进MMP-1和MMP-14分泌,提高血清MMP-1水平,从而减少ECM沉积。间充质干细胞通过降低整合素表达,阻断sFRP2及其下游靶点Axin2,促进血管生成,介导ECM重排。
细胞外囊泡的作用机制:通过RNA(尤其是miRNA)和蛋白质的装载发挥营养和调节作用。通过表面相互作用被受体细胞吸收,并可能通过基于蛋白质的网络发挥作用。局部给药在靶细胞中达到较高的浓度,具有两期分布和体内清除。
本文对肝硬化和肝纤维化的干细胞治疗进行了全面概述。它强调了干细胞发挥治疗作用的多种机制。利用细胞外囊泡探索无细胞治疗为更安全的治疗提供了一条有希望的途径,尽管标准化EV提取方法等挑战仍然存在。来自干扰素- γ预处理细胞的细胞外囊泡在缓解炎症和纤维化方面的有效性强调了综合方法对增强治疗结果的重要性。尽管面临持续的挑战,但这些发现为推进肝脏疾病的干细胞治疗提供了有价值的见解。
-END-
素材源于网络,内容有改动
版权归原作者所有,侵删!
【北联干细胞-iPSC细胞实验室】
— 感谢 · 阅读 —
北京北联世纪干细胞生物科技有限公司,是一所集临床、科研、国际学术交流为一体的全球生命科学研究公司,技术源头为美国圣地亚哥Biocentrium公司,公司致力于再生医学新技术的基础研究与临床应用转化,并将iPSc诱导多能干细胞培养技术平移到国内,同时与国内多家三甲医院开展科研课题。
现涵盖iPSc诱导多能干细胞,鲜活细胞、间充质干细胞、神经干细胞、血管内皮干细胞、软骨干细胞、NK/NKT/CTL/CAR-T/CAR-NK/DC-CIK/INKT等免疫细胞,肿瘤疫苗等;应用范围包括:疾病预防、两性生殖、神经系统疾病、脑部疾病、亚健康、免疫系统疾病、骨关节疾病等,同时拥有个体化iPS制备和分化成精原细胞、卵原细胞并形成精子、卵子技术、NSC脑部立体定向技术、NSC球后视神经靶向技术等。
-

-
被誉为“细胞导弹”的CIK免疫细胞疗法到底有什么特殊的作用
一、免疫失衡是癌症发生发展元凶免疫功能对身体的重要性,尤其是对癌症患者的重要性早已不言而喻,人类患病的最终根源都可以归结于免疫功能的异常。让
-
-
带你了解什么是人羊膜干细胞?以及它的特点和临床进展
人类生于细胞、老于细胞、死于细胞。干细胞来源广泛,骨髓来源、脂肪来源、牙髓来源、围产期组织来源,均可获得丰富的干细胞。而围产期组织来源中,除
-
脑外伤后遗症能治好吗?
脑外伤后遗症能治好吗?能用神经干细胞来治疗吗?赵医生 心脑血管科
脑外伤后遗症最有效的方法?
赵医生 心脑血管科
